2025年1月28日,我院汪香婷课题组与刘连新课题组合作,在The EMBO Journal发表了题为“Micropeptide hSPAR regulates glutamine levels and suppresses mammary tumor growth via a TRIM21-P27KIP1-mTOR axis”的研究论文。

长链非编码RNA(lncRNA)是一类在多种生理病理过程中发挥调控作用且长度不小于200核苷酸的转录产物。汪香婷课题组长期从事lncRNA的功能与机制研究,并在此领域取得了显著成果。近年来,课题组报道了多条具有独特功能调控机制的lncRNA分子,包括调控小脑突触完整性和运动功能的lncRNA-PM(Promoting Methylation)、调控肿瘤pH稳态的lncRNA-LINC00887、促进微管组装的lncRNA-TubAR(tubulin-associated lncRNA)。
近年来的研究发现,大约有40 %的lncRNA具有编码氨基酸产物的潜能。这些氨基酸产物通常不超过100个氨基酸,但却以丰富的调控机制广泛参与了植物生长、胚胎发育、免疫调节、肌肉组织的分化与再生和肿瘤的发生发展,被统称为微蛋白或者微肽。
2017年,哈佛医学院的Pier Paolo Pandolfi课题组发现由lncRNA LINC00961编码的微蛋白 SPAR(small regulatory polypeptide of amino acid response)在哺乳动物中具有较高的保守性,且在阻止小鼠肌肉细胞的分化和再生的过程中发挥着重要的作用。然而,SPAR在人类疾病发生发展中的作用仍尚不明确。
mTOR信号通路在真核细胞的生长和代谢过程中扮演着关键角色。现有的研究表明,该信号通路受到营养、能量状态以及生长因子等多种因素的调控。2020年,图卢兹大学的 Arnaud Besson研究团队首次揭示在营养限制条件下,细胞周期负调控因子P27KIP1转运至溶酶体膜上,进而抑制mTOR信号通路的激活。然而,目前尚未明确调控P27KIP1向溶酶体膜转移的具体分子机制及其如何影响mTOR信号通路活性的详细过程。
汪香婷课题组与合作团队的论文发表,在国际上首次报道了人源 SPAR(Human SPAR,hSPAR)抑制肿瘤增殖的作用,并详细解析了hSPAR通过其肿瘤谷氨酰胺代谢调控因子等作用而在三阴性乳腺癌中抑制mTOR信号通路激活的分子机制。
在本项工作中,研究人员证明hSPAR具有抑制乳腺癌细胞生长和增殖的抗肿瘤效应。利用乳腺癌细胞和小鼠移植瘤模型,该研究进一步证明了hSPAR通过协同促进P27KIP1的表达和溶酶体定位而抑制 mTOR信号通路的分子机制。
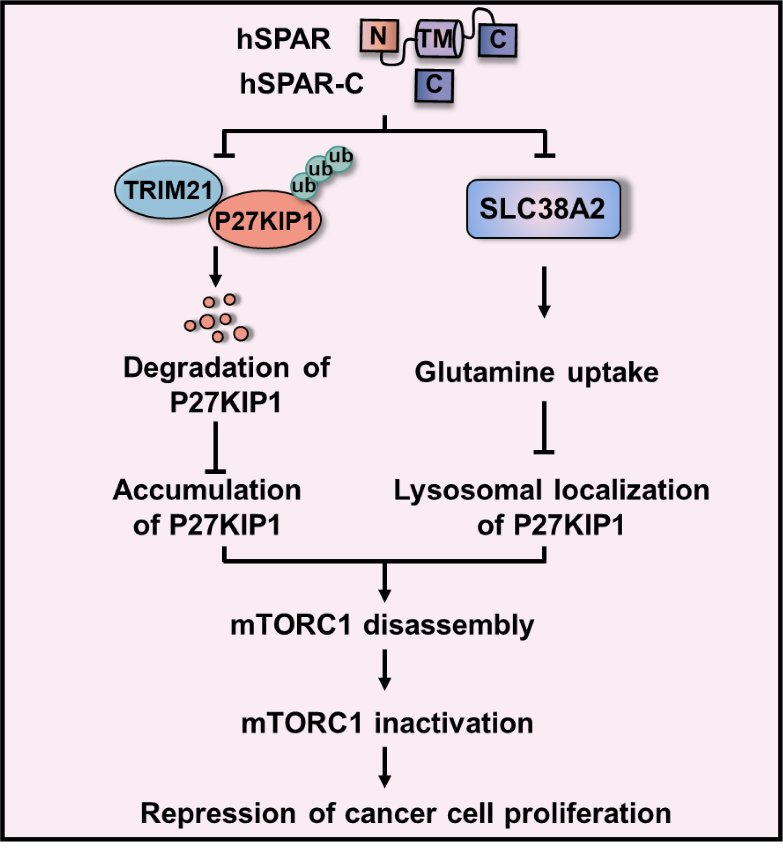
图一:hSPAR通过TRIM21/谷氨酰胺缺失- P27KIP1途径协同调控mTOR活性,
抑制三阴性乳腺癌的生长
本项研究发现hSPAR/hSPAR-C通过协同促进P27KIP1的表达及其溶酶体定位,强烈地抑制了mTOR信号通路的激活和三阴性乳腺癌细胞的增殖。该研究揭示了由微蛋白介导的肿瘤氨基酸代谢对非经典 P27KIP1-mTOR通路调控的作用,并为乳腺癌的诊断和治疗提供了新的标记物和靶点。
中国科学技术大学附属第一医院(安徽省立医院)及生命科学与医学部博士研究生黄炎为该研究的第一作者,中国科学技术大学附属第一医院(安徽省立医院)汪香婷研究员、刘连新教授和安徽师范大学的申涛副教授为该工作的共同通讯作者。该研究也得到昆明医科大学陈策实研究员和北京大学崔庆华教授的支持。(老年医学研究所 汪香婷 文/图 许秀文 刘尧/审核)
责编:吴家炜
原文链接:https://www.embopress.org/doi/full/10.1038/s44318-024-00359-z