发布日期:2026-05-13 10:20 来源:内分泌代谢科 作者:骆斯慧、耿梦雅 点击:361
近日,中国科学技术大学翁建平、刘连新教授团队在脂肪肝研究领域取得重大突破,首次揭示了干扰素相关发育调节因子1(IFRD1)通过调控谷氨酸脱氢酶1(GLUD1)介导的α-酮戊二酸(α-KG)生成,形成代谢-表观遗传调控轴抑制肝脏从头脂肪生成(DNL)的分子机制,为代谢功能障碍相关脂肪性肝病(MASLD)的精准治疗提供了新靶点与策略。相关研究成果以“Hepatic IFRD1 suppresses metabolic dysfunction-associated fatty liver disease via GLUD1/α-KG axis”为题发表在《Science Bulletin》(《科学通报》)上。
MASLD作为当前全球发病率最高的慢性肝病,已成为严重威胁人类健康的公共卫生问题。该病可从单纯的肝脏脂肪变性逐步进展为代谢相关脂肪性肝炎、肝硬化,甚至诱发肝细胞癌,但其病理机制复杂,尤其是代谢重塑与表观遗传修饰的关联尚未完全阐明,临床治疗缺乏特效靶点。其中,肝脏从头脂肪生成(DNL)的异常激活被认为是MASLD发病的核心病理特征,也是该领域药物研发的关键方向。
中科大研究团队通过临床样本分析与多种小鼠模型实验,取得三项关键创新发现:一是明确IFRD1的疾病保护作用。团队证实,人肝组织中IFRD1表达水平与MASLD疾病进展呈显著负相关;敲除该因子会加重小鼠MASLD病理表型,肝细胞特异性过表达则能有效遏制病情发展。二是解析全新分子调控机制。IFRD1可结合谷氨酸脱氢酶1(GLUD1)特定氨基酸位点,促进其线粒体定位并稳定酶活性,进而增加α-酮戊二酸(α-KG)的生成;α-KG通过表观遗传调控降低脂肪生成相关基因的甲基化修饰,直接抑制肝脏从头脂肪生成。三是验证干预策略的转化潜力。外源性补充α-KG可有效逆转IFRD1敲除小鼠的MASLD加重表型;更为重要的是,临床样本分析证实,MASLD患者肝脏中GLUD1酶活性、α-KG含量显著降低,相关基因甲基化水平升高,且这些指标与IFRD1表达呈显著负相关,证实该调控轴在人类发病中同样关键。
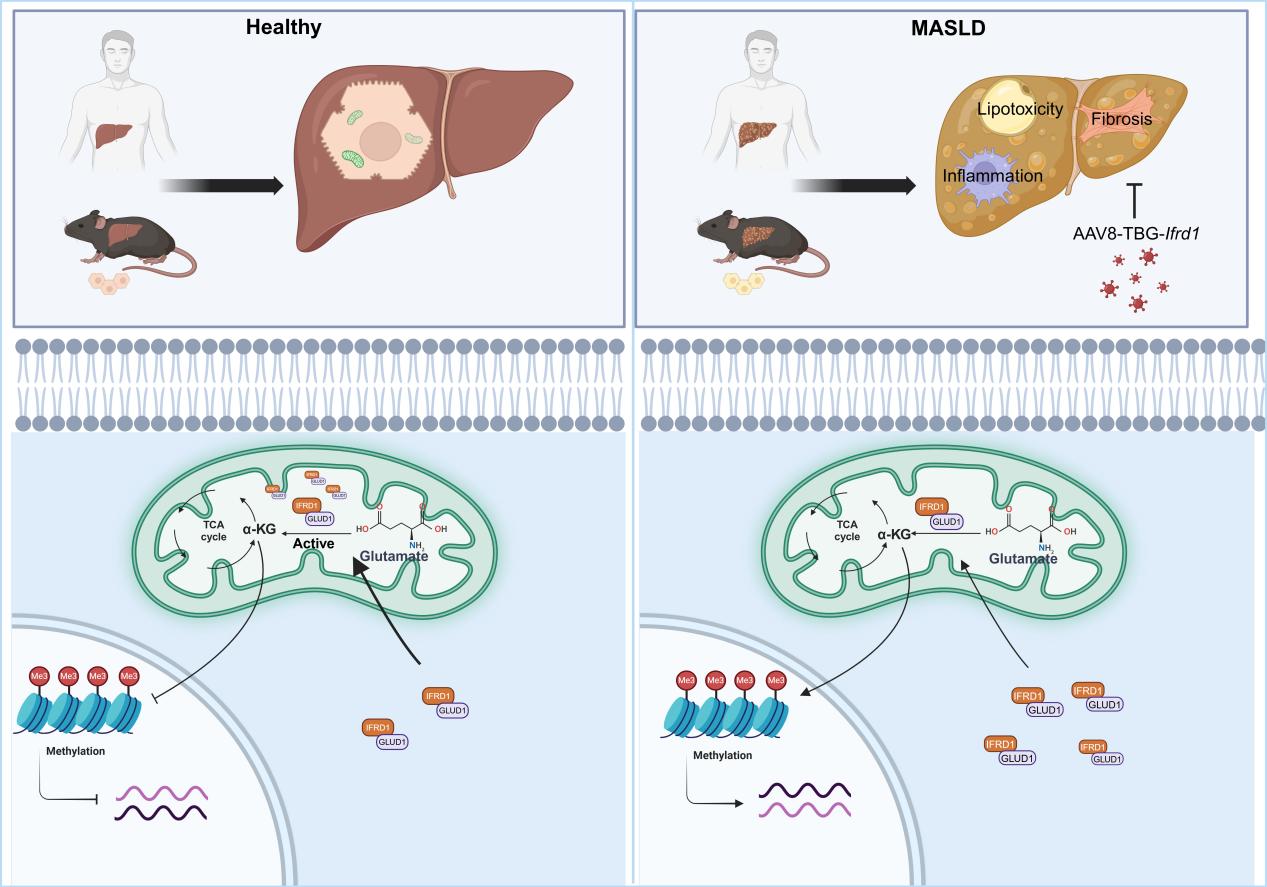
该研究系统阐明了IFRD1-GLUD1-α-KG轴是连接代谢调控与表观遗传修饰的关键通路,不仅首次建立了IFRD1与MASLD进展的临床关联,还揭示了GLUD1酶活性参与调控MASLD的新机制,验证了代谢中间体α-KG的表观遗传调控作用,为MASLD的“代谢—表观遗传”靶向治疗开辟了新范式。
耿梦雅、孟凡征、李海瑞、孙礼洁为文章的第一作者,刘连新、翁建平、骆斯慧为共同通讯作者。该工作得到了国家自然科学基金、中国科学技术大学附属第一医院临床转化研究专项、中国科学技术大学附属第一医院创新研究团队项目、安徽省教育厅项目的资助。
论文链接:https://www.sciencedirect.com/science/article/pii/S2095927326003658
(内分泌代谢科 骆斯慧、耿梦雅/文 刘尧/审核)
责编:方雯


微信扫一扫
关注公众号

微信扫一扫
进入互联网医院

支付宝扫码
预约挂号
地址 :安徽省合肥市庐阳区庐江路17号
邮编 : 230001
地址 :安徽省合肥市政务文化新区天鹅湖路1号
邮编 : 230036
地址 :安徽省合肥市蜀山区环湖东路107号
邮编 : 230031
地址 :安徽省合肥市长丰县阜阳北路与龙湖路交叉路口西北角
邮编 : 231131
 皖公网安备34010302001040号Designed by MingGao
皖公网安备34010302001040号Designed by MingGao